NEB 發(fā)布:GenomONE? 為誘導 iPSC 形成「保駕護航」
發(fā)布人:admin
瀏覽次數:1447
發(fā)布時(shí)間:2017-11-15
間充質(zhì)干細胞(MSC, mesenchymal stem cells)是干細胞家族的重要成員�����,屬于多能干細胞�,因其具有多向分化潛能��、造血支持和促進(jìn)干細胞植入�����、免疫調控和自我復制等特點(diǎn)而日益受到人們的關(guān)注��。誘導性多能性的間充質(zhì)干細胞(iPMSCs)是藥物篩選�����、再生醫學(xué)和細胞治療的新型候選藥物���。然而�����,用于生成骨髓間充質(zhì)干細胞的誘導性多能性間充質(zhì)干細胞(iPSC)����,在導入編碼基因的轉錄因子中���,往往伴隨有在靶細胞基因組的插入時(shí)發(fā)生突變的風(fēng)險�。
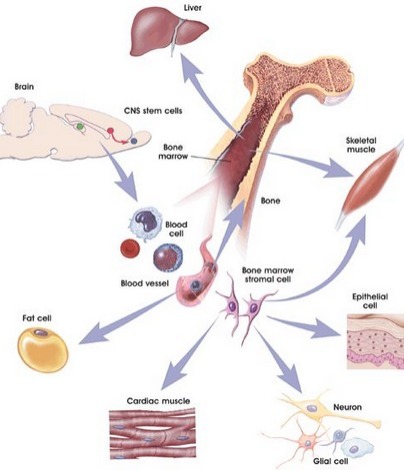
由于近年來(lái)對骨髓間充質(zhì)干細胞認知地深入��,在造血系統����、免疫系統中的重要作用�,怎么樣能高效地��,精準地利用誘導性多能性間充質(zhì)干細胞(iPSC)生成骨髓間充質(zhì)干細胞呢���?研究發(fā)現使用滅活的病毒顆粒�,包裝和表達四個(gè)純化重組 Yamanaka 轉錄因子(Sox2����、Oct4����,Klf4 和 c-Myc)����,從而引起人初級成纖維細胞的重編程�。全基因組亞硫酸鹽測序分析人類(lèi) iPMSCs 的全基因組 CpG 甲基化�����。使用 Western blot�����、熒光定量 PCR���、免疫熒光����,和體外分化評估 iPMSCs 的多能性��。結果表明這些 iPS 細胞在體外和體內都成功分化成三個(gè)胚層的細胞�����。在本研究中分化誘導后���,表達的轉錄因子被降解����,從而改善后續程序分化的效率�����。由此可見(jiàn)��,iPMSC 的重編程和衍生的重組轉錄因子提供了患者細胞再生醫學(xué)的一種高效新方法����。
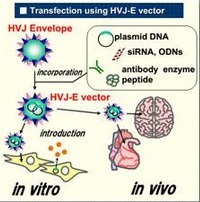
高效新方法的發(fā)現���,完全歸功于滅活的病毒顆?�!膳_病毒包膜�。請注意三點(diǎn):滅活��、病毒����、包膜�����。具體來(lái)說(shuō)��,滅活使其無(wú)毒性����,病毒衣殼蛋白的侵染能力����,包膜的融合蛋白�����。也就是這三點(diǎn)作用機制���,使得仙臺病毒包膜可以高效地���,精準地轉染細胞�,從而完成相關(guān)誘導���。
(本文轉載丁香通)






