我國學(xué)者在烷烴碳氫鍵不對稱(chēng)官能化領(lǐng)域取得重要進(jìn)展
發(fā)布人:admin
瀏覽次數:1156
發(fā)布時(shí)間:2016-09-12
日前��,中國科學(xué)院上海有機化學(xué)研究所劉國生課題組與美國威斯康辛大學(xué)麥迪遜分校的Stahl教授合作���,在基于自由基策略的碳氫鍵不對稱(chēng)官能化研究方面取得重要進(jìn)展���,高選擇性地合成了光學(xué)活性腈類(lèi)化合物�。該研究發(fā)展的新策略充分結合了自由基化學(xué)的高活性和金屬催化的高選擇性�,成功地解決了無(wú)輔助配位條件下烷烴碳氫鍵的不對稱(chēng)氰化反應�����,不僅為不對稱(chēng)自由基反應的研究提供了新的反應模式�����,而且為后期進(jìn)一步研究烷烴的不對稱(chēng)官能化反應提供了新思路��。相關(guān)研究成果以Enantioselective cyanation of benzylic C–H bonds via copper-catalyzed radical relay(銅催化/自由基接力的芐位C-H鍵對映選擇性氰化反應)為題于2016年9月2日在Science發(fā)表�。該研究工作得到了國家杰出青年科學(xué)基金(項目編號:21225210)和國家自然科學(xué)基金重點(diǎn)項目(項目編號:21532009)等項目的支持���。
碳氫鍵活化是有機化學(xué)的重大挑戰領(lǐng)域之一����。通過(guò)烷烴/芳烴的碳氫鍵直接官能化是合成有機化合物最為直接高效的新方法�����,但是在反應活性和選擇性等方面存在諸多問(wèn)題���,碳氫鍵的不對稱(chēng)催化尤為困難����。目前該領(lǐng)域的研究主要是利用過(guò)渡金屬活化碳氫鍵的策略���,并通過(guò)定位基團的輔助實(shí)現碳氫鍵不對稱(chēng)官能化��。但該策略對于普通(無(wú)定位基團)芳/烷烴而言���,碳氫鍵活化及其不對稱(chēng)催化一直沒(méi)有得到有效解決�。相對而言�,受酶化學(xué)的啟發(fā)而發(fā)展的自由基策略是普通烷烴碳氫鍵官能化的一種非常有效的途徑�����;但反應所涉及的碳自由基中間體具有很高的活性�����,導致反應的選擇性控制非常困難���,基于該策略來(lái)發(fā)展碳氫鍵不對稱(chēng)官能化鮮見(jiàn)報道���。
劉國生課題組近年來(lái)致力于自由基化學(xué)的選擇性控制方面的研究���,他們提出將反應中的碳自由基中間體轉化為金屬有機物種來(lái)實(shí)現選擇性控制的策略�,籍此來(lái)解決烷烴的C-H鍵不對稱(chēng)直接官能化的難點(diǎn)問(wèn)題����。他們首先利用該策略對烯烴的選擇性雙官能化反應展開(kāi)了系統的研究���,成功地實(shí)現了菲啰啉/鈀絡(luò )合物對碳自由基氟化反應的選擇性調控���,發(fā)展了高立體選擇性的烯烴氟砜化反應(J. Am. Chem. Soc., 2015, 137, 2468)����。在進(jìn)一步探索不對稱(chēng)自由基反應的過(guò)程中��,研究人員發(fā)現手性噁唑啉/銅氰絡(luò )合物可以很好與碳自由基進(jìn)行立體專(zhuān)一性的結合�,形成高活性的有機金屬銅中間體�,通過(guò)金屬中心高立體選擇性的還原消除�,實(shí)現了碳自由基的不對稱(chēng)控制�����,發(fā)展了烯烴的不對稱(chēng)氰化反應����。
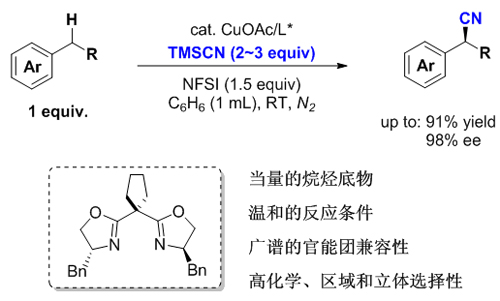
在以上工作的基礎上��,他們對更具挑戰性的烷烴碳氫鍵的不對稱(chēng)官能化展開(kāi)了研究�,發(fā)展了金屬催化/自由基接力的新策略��。研究人員通過(guò)原位形成的高活性的自由基來(lái)攫取芐位的氫���,在溫和條件下生成的芐位自由基與手性噁唑啉/銅氰絡(luò )合物反應���,成功地實(shí)現了芐位碳氫鍵的不對稱(chēng)氰化反應����,無(wú)需鄰位定位基團的參與就可以實(shí)現從芐位碳氫鍵到手性芳基乙腈的直接高效轉化��。該反應具有廣譜的官能團兼容性和出色的化學(xué)�、區域和立體選擇性���,以最短的路線(xiàn)��、高效地制備了各種光學(xué)純腈類(lèi)化合物����。腈類(lèi)化合物是一類(lèi)非常重要的有機中間體����,可以轉化為相應的胺類(lèi)�����、以及羧酸等化合物����,被廣泛地應用于醫藥��、農藥和材料等領(lǐng)域���。